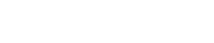Существует многочисленные методы определение фенолов в различных веществ [ 1, 230с ]. Представленный метод относится к определению малых содержаний фенола, выделяющихся водяным паром при различных условиях. Метод основных образовании ионов диазототированный сульфаниловой кислотой оранжево- желтового цвета при исследовании водных образцов [ 2 ]. Диазотированием сульфоналиновый кислоты и образовании в щелочной среды оранжего- желтого цвета протекает по реакции:
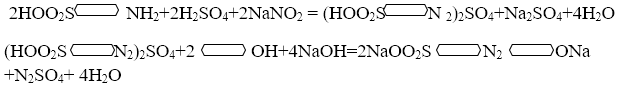
В исследовании использованы грунтовая вода Сабунчинского района Абшеронского полуострова (АР). Образцы воды отфильтрованы беззольного фильтра «белая лента», отделены от механических примесей, нефтепродуктов, эмульции и мутности. При этом было учтены метастабильность водного раствора фенолов [3, с.19]
Диазотизации сульфаниловой кислоты производят смещением трех растворов. Сначала 1,91г. перекристализированная сульфониловая кислота и 0,85г. химических чистый азотистокислый натрий в отдельности растворяется по 250 мл дистиллированной воде, а концентрированная серная кислота разбавляют водой при соотношении в 1:3 соответственно. Затем 5 объем раствора сульфаниловой кислоты в условиях охлаждение смешивают равным объемом разбавленной сериой кислотой, затем добавляют 5 объем раствора азотистокислый натрий. Раствор гидрооксид натрия получают растворением 10 г NаОН в 90 мл дистиллированной воде.
С целью определения фенола стандартный раствор приготавливаются следующим образом: 2г. хлорплатинат калий растворяется 100 мл концентрированной соляной кислоте и объем доводят дистиллированной водой до одного литра, тщательного смешивают (основной раствор). Из основного раствора берут 2,2; 3,8; 4,5; 5,5; 7,0; 10,0 и 17,0мл и разбавляют дистиллированной водой в цилиндре и объем доводят до 100 мл. В указанных растворах содержание фенола составляет 0,001; 0,003; 0,005; 0,07; 0,10; 0,020; 0,030 мг соответственно.
Учитывая, что хлорплатинат калия в настоящее время является дефицитном реактивом, альтернативом было использовано раствор самого фенола. Для этого 1г фенол растворяется в 1 л дистиллированной воде. Туда же добавляют 2,5 мл диазотированную сульфаниловую кислоту и разбавляют 2,5 мл раствором гидрокисидом натрия. Затем полученном цвет раствора сравнивают исследованными раствором.
Алгоритм выполнение измерений: исследованный образец 250 мл воды подкисляют 3-5 мл серной кислотой и перегоняют в лабораторном установке водяным паром. Конец перегонки фенола определяется путем приема пробирки из раствора с последующем добавлением диазтированной смесью. Перегоняемый раствор переводят в 250 мл мерную колбу, объем доводят дистиллированной водой до метки.
В 100 мл цилиндре берут из этого раствора и туда же добавляют 2,5 мл свежеприготовленный раствор диазотированной сульфаниловой кислоты и 2,5 мл раствор NaOH. Раствор перемешивают стеклянной палочкой и дают отстоят на 5 минут. Цвет полученного раствора сравнивают стандартным раствором и определяют содержание фенола по ниже указанной формулой.
![]()
где; С- содержание фенола в ислсдуемой воды, мг/л; а –содержание фенола в эталонном растворе, мг/л; – количество анализируемой воды, мл.
В случае, когда перегоняемой объем воды равняется объему анализируемой воды ![]() формула имеет следующий вид;
формула имеет следующий вид;
![]()
Проводимые нами параллельные анализы показал хорошие сходимости результатов и относительные погрешность составляет не более 7-9%.
ЛИТЕРАТУРА
- Каплин В.Т., Фисенко И.Г., Методы анализа органических веществ в природных и сточных водах. М.1972,230с.
- Шапиро С.А., О содержании фенолов в воде источника Нафтуся. УХЖ, т.17, вып.4,1991
- Лурье Ю.Ю., Рыбников А.И., Химический анализ производственных сточных вод , М. Химия, 1987,334с.